Grundlagen Redox
Wie der Name schon sagt, handelt es sich bei einer Redoxreaktion sowohl um eine Reduktion wie auch um eine Oxidation. Dabei verliert ein Atom ein Elektron (Oxidation) welches von einem anderen Atom angezogen wird (Reduktion).
Inhaltsverzeichnis
Einführung Teilgleichungen Oxidation, Reduktion
Exp. Brom mit Aluminium

Ein Reagenzglas wird zur Hälfte mit Brom gefüllt, danach wird Alufolie hinzugegeben. Das Experiment sollte unter einer Abzugshaube durchgeführt werden, um die unangenehmen Dämpfe abzusaugen. Die Reaktion braucht anfangs etwas Zeit bis sie ins Laufen kommt, danach ist sie jedoch heftig.
Darstellung
Reaktionsgleichung: 2Al + 3Br2 → 2Al3+Br-3
Nun kann die die ganze Reaktionsgleichung in zwei Teilgleichungen unterteilt werden.
Oxidation: Al → Al3+ + 3e-
Reduktion: Br2+ 2e- → 2Br-
Die Elektronen werden jeweils auf der Seite hinzugeschrieben auf der sie positiv dargestellt werden können. Da Aluminium beim Produkt Elektronen fehlen werden sie auf der Produktseite einfach wieder hinzugeschrieben. Aluminium hat im Periodensystem die Oxidationszahl III daher werden 3 Elektronen dazugeschrieben. Brom hat die Oxidationszahl -I und da es zwei Bromatome sind werden hier 2 Elektronen hinzugefügt. Nun müssen die beiden Teilgeleichungen so ausgeglichen werden, dass Aluminium so viele Elektronen abgibt wie Brom aufnimmt. Das kleinste gemeinsame Vielfache von 2 und 3 ist 6. Also wird die Oxidation mit 2, und die Reduktion mit 3 multipliziert.
Oxidation: 2Al → 2Al3+ + 6e-
Reduktion: 3Br2 + 6e- → 6Br-
Aus diesen angepassten Teilgeleichungen kann nun wieder auf die ganze Reaktionsgleichung vom Anfang geschlossen werden.
Oxidationszahlen bei Molekülen
Am Beispiel: CH4 + 2O2 → CO2 + 2H2O
Ein ganzes Molekül kann in dem Sinn nicht oxidieren, nur die jeweiligen einzelnen Atome. Daher muss von jedem Atom einzeln die Oxidationszahl ermittelt werden. Mit Hilfe der Elektronegativität kann bestimmt werden, welche Atome Elektronen verlieren (also oxidieren) und welche Atome Elektronen aufnehmen.
CH4 zum Beispiel: C hat, wie im Periodensystem nachgesehen werden kann, eine Elektronegativität von 2,5. H dagegen eine von 2,1. Da C elektronegativer ist klaut es die Elektronen und zwar nach Oxidationszahl IV. H dagegen hat die Oxidationszahl -I, da es vier sind werden diese vier vom C-Atom aufgenommen. Wird dies nun mit allen einzelnen Atomen gemacht, kommt man auf folgende Reaktionsgleichung:
C-IVH4+IV + 2O20 → C+IVO2-IV + 2H2+IIO-II
Oxidation: Alle Atome die einen Verlust von Elektronen haben, die Oxidationszahl vom Edukt zum Produkt also positiver wird. Das C-Atom gehört zur Oxidation weil es beim Edukt die Oxidationszahl -IV hat beim Produkt jedoch +IV
C-IV → C+IV + 8e-
Reduktion: Alle Atome die Elektronen stehlen, die Oxidationszahl vom Edukt zum Produkt also negativer wird. Dies ist hier der Fall beim Sauerstoffatom.
O20 + 4e- → 2O-II
Nun wird die Gleichung wiederum angepasst. Das kleinste gemeinsame Vielfache von vier und acht ist acht. Also muss die Reduktionsgleichung mit zwei multipliziert werden.
Oxidation: C-IV → C+IV + 8e-
Reduktion: 2O20 + 8e- → 4O-II
Hat die gesamte Reaktionsgleichung keine Änderungen der Oxidationszahlen von Edukt zum Produkt der einzelnen Atome, handelt es sich um KEINE Redoxreaktion.
Komplexe Moleküle
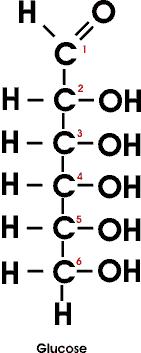
Am Beispiel der Photosynthese: 6CO2 + 6H2O → C6H12O6 + 6O2
Versieht man nun wiederum alle einzelnen Atome mit der Elektronegativität und fügt die Oxidationszahlen hinzu wird es etwas komplizierter. Beim komplexen Molekül C6H12O6 wäre die Oxidationszahl für ein C-Atom laut PS +IV, was insgesamt dann 24 wären. Da ein Molekül aber immer auf die gesamt Oxidationszahl 0 kommen muss und H und O zusammen bereits 0 ergeben kann dies nicht sein. Betrachtet man das Molekül genauer, sieht man warum. Die mittleren C-Atome haben eine Oxidationszahl von null (Bild C-Atome 2-4), die beiden an der Seite jedoch haben die Oxidationszahl I bzw. -I. Somit kommen wir auf einen Durchschnitt der Oxidationszahl von 0, was aufgeht. Ist ein Molekül also komplexer und enthält mehrere C-Atome müssen diese einzeln betrachtet werden.
6C+IVO2-IV + 6H2+IIO-II → C60H12+XIIO6-XII + 6O20
Oxidation: 12O-II → 6O20 + 24e-
Reduktion: Einzelne C-Atome aufschreiben und Elektronen zusammenzählen gibt auch wieder 24 Elektronen.
C+IV + 5e- → C-I
4C+IV + 16e- → 4C0
C+IV + 3e- → C+I
Regeln und Hilfsregeln
Regeln
1. Die Oxidationszahlen (OxZ) werden mit römischen Ziffern bezeichnet und können meist im PS nachgesehen werden.
2. Bei einatomigen Ionen ist die OxZ gleich der Ionenladung: Na+IO-II
3. In Molekülen werden die Bindungselektronen dem Bindungspartner mit der höheren Elektronegativität zugeordnet. Die sich so ergebenden "Ladungen" entsprechen den Oxidationszahlen.
4. Die Oxidationszahlen der Elemente sind definitionsgemäss gleich Null.
Hilfsregeln
1. Die Summe der Oxidationszahlen aller Atome in einem Molekül ist gleich Null
2. Die Summe der Oxidationszahlen aller Atome in einem mehratomigen Ion ist gleich der Ladung des Ions.
3. Die OxZ von Sauerstoff in Verbindungen ist meist -II aufgrund der hohen Elektronegativität. Ausnahmen: Wasserstoffperoxide (H2O2) und Bindungen mit Fluor (F2O)
4. Die OxZ von Wasserstoff in Verbindungen ist meist +I aufgrund der tiefen Elektronegativität. Ausnahme: Metallhydride.
5. Bei komplexeren Molekülen in denen mehrere C-Atome enthalten sind, müssen diese einzeln betrachtet werden. Bsp: 6CO2 + 6H2O → C6H12O6 + 6O2
Quellen
- Chemieunterlagen