Der Einfluss der Enthalpie ∆H auf die Freiwilligkeit
Inhaltsverzeichnis
- 1 Repetition: Definition von ΔH
- 2 Warum gibt es freiwillige und unfreiwillige Reaktionen?
- 3 Warum verlaufen sehr viele exotherme Reaktionen freiwillig?
- 4 Warum wird es immer warm bei exothermen Reaktionen?
- 5 Hypothese von Berthelot
- 6 Zufällige Teilchenbewegung
- 7 Exkurs kinetisches und thermodynamisches Produkt
- 8 Quellen
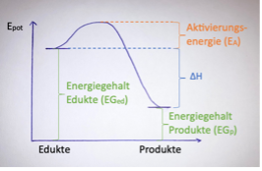
Repetition: Definition von ΔH
ΔH ist die Energie, die bei einer chemischen Reaktion frei wird, beziehungsweise aufgewendet werden muss. Die Bedingung dafür ist, dass die Reaktion isobar und isotherm verläuft, also dass der Druck und die Temperatur konstant bleiben.
Warum gibt es freiwillige und unfreiwillige Reaktionen?
Chemische Stoffe besitzen von Natur aus eine gewisse Energiemenge. Diese Energie kann entweder ausreichen, um eine Reaktion zum Ablauf zu bringen, oder nicht. Während einer Reaktion kann die chemische Energie dabei in Wärme umgewandelt werden.
Chemische Reaktionen werden je nach ihrer Spontanität beziehungsweise Freiwilligkeit in zwei Gruppen unterteilt: freiwillige und unfreiwillige Reaktionen.
Freiwillige Reaktionen treten von selbst auf. Es muss keine externe Energie hinzugefügt werden und diese Reaktionen sind dadurch gekennzeichnet, dass sie zu einer Abnahme der Energie im gesamten chemischen Reaktionssystem führen. Ein Beispiel dafür ist das Rosten von Eisen. Eisen reagiert dabei mit dem Sauerstoff aus der Luft und bildet Rost, ohne dass extern hinzugefügte Energie erforderlich ist.
Unfreiwillige Reaktionen brauchen eine externe Energiequelle, damit sie ablaufen können. Diese Reaktionen führen zu einer Zunahme der Energie im System. Ein geeignetes Beispiel dafür ist die Elektrolyse von Wasser. Bei dieser Reaktion wird Wasser nur dann in Wasserstoff und Sauerstoff zerlegt, wenn elektrische Energie zugeführt wird.
Freiwillige Reaktionen geschehen, weil sie energetisch günstig sind. Unfreiwillige Reaktionen brauchen hingegen Energiezufuhr von aussen.
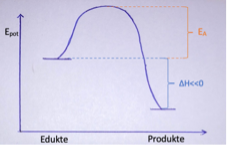
Warum verlaufen sehr viele exotherme Reaktionen freiwillig?
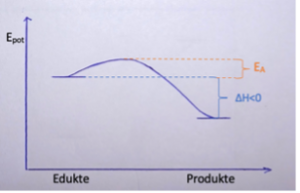
Exotherme Reaktion
Wenn energiereiche Stoffe freiwillig zu energiearmen Stoffen reagieren, wird Energie beispielsweise in Form von Wärme frei. Es handelt sich dabei um exotherme Reaktionen.
ΔH<0
ΔH wird wie folgt berechnet: ΔH = EGp - EGed
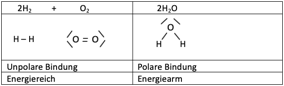
Analyse der Bindungskräfte bei Knallgasreaktionen:
2H2 + O2 → 2H2O
Wenn unpolare, energiereiche Bindungen zu polaren, energiearmen Bindungen werden, ist ΔH<0.
Eine weitere wichtige Erkenntnis ist, dass Steine stets nach unten rollen.
Steine rollen nach unten, da die potenzielle Energie (Epot) durch die Gravitationskraft in kinetische Energie (Ekin) umgewandelt wird, sodass ein Zustand minimaler Energie erreicht wird.
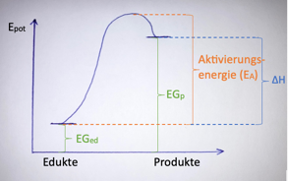
Endotherme Reaktion
Wenn Energie aufgewendet oder von der Umgebung hinzugefügt werden muss, damit energetisch tieferliegende Edukte zu energiereicheren Stoffen reagieren, kühlt sich die Umgebungstemperatur ab. Es handelt sich dabei um eine endotherme Reaktion.
ΔH>0
ΔH wird wie folgt berechnet: ΔH = EGp - EGed
Warum wird es immer warm bei exothermen Reaktionen?
Exotherme Reaktionen in Lebewesen verursachen im Vergleich zu Umgebung erhöhte Körpertemperatur, da ständig Edukte in Produkte umgewandelt werden. Ein Beispiel dafür ist die Muskelkontraktion, bei welcher aus ATP, ADP und Phosphat entsteht. Die Erhöhung der Körpertemperatur geschieht, da die Energie der Produkte geringer ist als die der Edukte. Ein anderes Beispiel sind Gärvorgänge, bei denen Wärme an die Umgebung abgegeben wird. Aufgrund dieser Beispiele kann man vermuten, dass die Reaktionsenthalpie ΔH entscheidend ist für die Freiwilligkeit chemischer Reaktionen. Bei diesen Reaktionen wird elektrische Energie (Epot) in Bewegungsenergie (Ekin) umgewandelt und es entsteht Wärme. Epot → Ekin → Wärme
Und genau das hat Marcellin Berthelot 1878 formuliert und es entstand das «Prinzip von Berthelot».
Hypothese von Berthelot
Marcellin Berthelot formulierte das Prinzip von Berthelot: Jede chemische Reaktion, die in einem abgeschlossenen System, also ohne Einflüsse von äusserer Energie abläuft, will das Produkt oder den Körper bilden, welches am meisten Wärme freisetzt.
Freiwillige Reaktionen sind exotherm und die Temperatur steigt.
Unfreiwillige Reaktionen sind endotherm und die Temperatur sinkt.
Überprüfung der Hypothese
Falsifizierung: Aber es gibt auch freiwillige endotherme Reaktionen?
Für eine Falsifizierung wird grundsätzlich nur ein Gegenbeispiel benötigt.
1. Verdunsten von H2O(l) zu H2O(g) → ΔH>0, freiwillig
Temperatur sinkt schnell und stark
Somit ist Verdunsten von H2O eine freiwillige und endotherme Reaktion.
2. Bariumhydroxid: Ba(OH)2 und Ammoniumthiocyanat: NH4SCN
Werden diese zwei Salze zusammengeschüttet, sinkt die Temperatur → ΔH>0, freiwillig
Somit ist es eine freiwillige und endotherme Reaktion.
Tabelle
Ein Video dieser Reaktion zum besseren Verständnis:
Zufällige Teilchenbewegung
Die zufällige Teilchenbewegung spielt eine wichtige Rolle für den freiwilligen Verlauf chemischer Reaktionen. Ionen zittern, stossen zufällig zusammen und durch starke Stösse entfernen sie sich voneinander und aus dem Gitter hinaus. Dies zeigt sich gut am Beispiel eines endothermen Lösevorgangs eines Salzes wie z.B. Ammoniumchlorid in Wasser. Ionen werden getrennt und von Wasser-Molekülen umgeben. Ist die Hydrationsenthalpie kleiner als die Gitterenergie, ist der Lösevorgang endotherm. Das Stoffsystem geht somit von einem energieärmeren in einen energiereicheren Zustand über und dies geschieht freiwillig.
Wenn ein Ion mit einem anderen Ion zusammenstosst und nach einem starken Stoss nochmals stark getroffen wird, gibt es zwei Möglichkeiten:
1. Entweder das Ion wird so getroffen, dass es wieder zurück auf seinen Platz gestossen wird und durch die Anziehungskräfte gehört es dann auch wieder zum Gitter
oder
2. Das Ion wird durch einen zusätzlichen Stoss weiter vom Gitter weggestossen und von Wasser-Molekülen umgeben und somit hydratisiert. Durch die Hydration werden die Anziehungskräfte zwischen dem Ionengitter und dem Ion geschwächt und das Ion entfernt sich noch weiter.
Es gibt viel mehr Möglichkeiten, dass Teilchen weiter weggestossen werden, als dass sie wieder zurück ins Gitter gespickt werden.
Fazit: Es geschieht das, was wahrscheinlich ist.
Mit der Anziehung zwischen den Teilchen und der Wahrscheinlichkeit kommen wir nun zum nächsten Thema und somit zur Entropie ΔS.
Hier gehts zu Die Entropie ΔS.
Exkurs kinetisches und thermodynamisches Produkt
Kinetisches Produkt:
- Niedrigere Aktivierungsenergie, verläuft deshalb schneller aber ist instabiler im Vergleich zum thermodynamischen Produkt.
Thermodynamisches Produkt:
- Stabiler, EA kann höher/grösser sein als beim kinetischen Produkt. Deshalb muss mehr Energie hinzugefügt werden, um das thermodynamische Produkt zu erhalten.
Bei niedrigen Temperaturen wird Aktivierungsenergie (EA) nur so gross, dass ein kinetisches Produkt entsteht. Bei höheren Temperaturen kann eine höhere Aktivierungsenergie erreicht werden und somit kann auch ein stabiles, thermodynamisches Produkt entstehen.
Quellen
- Chemieunterlagen
- Chemiebuch "Chemie für das Gymnasium - Günter Baars und Roger Deuber"