Das unfassbare Elektron
Der Name Elektron kommt vom griechischen Wort ηλεκτρόν was soviel bedeutet wie Bernstein, denn an ihm wurde die Elektrizität erstmals beobachtet.
Reibt man Bernstein beispielsweise mit einem Katzenfell, so lädt sich das Fell elektrisch auf. 1927 entdeckten Clinton Davisson & Lester Germer bei einem Experiment (siehe unten) die sogennanten Beugungsringe. Das Bedeutet, dass ein Elektorn nicht wirklich als ein Objekt im normalen Sinn betrachtet werden kann sondern eher als eine Welle betrachtet wird.
Inhaltsverzeichnis
Unfassbar
In der klassischen Physik
Was macht das Elektron so unfassbar? Bis heute ist man mit der Technik noch nicht im Stande, den Ort und die Geschwindigkeit gleichzeitig zu betimmen. Denn man hat herausgefunden, sobald man den einen Faktor genauer feststellt, wird der andere Faktor ungenauer. Das wird alles durch die Unschärferelationstheorie, die 1927 von Werner Heisenberg im Rahmen der Quantenmechanik formuliert wurde,erklärt.
∆p*∆q~h
∆p = Unschärfe der Geschwindigkeit (Impuls); ∆q = Unschärfe des Ortes; h = "Plancksches Wirkungsquantum
Ergibt ein konstantes Ergebnis, bei welchem, wenn man ∆p erhöht, sich ∆q verkleinert und umgekehrt.
Den Ort zu bestimmen ist sehr schwer, da sich die Teilchen unglaublich schnell bewegen. Wenn der Ort bestimmt ist, ist das Atom jedoch schon wieder an einem anderen Ort, es bleibt gar keine Zeit um die Geschwindigkeit irgendwie zu messen.
In der Quantenphysik
Es ist möglich beliebig genau die Wahrscheinlichkeit zu berechnen, wie gross die Wahrscheinlichkeit ist, ein Elektron an einem bestimmten Ort anzutreffen. Die Berechnung für die Wahrscheinlichkeit des Antreffens an einem bestimmten Ort des Elektrons kann mittels einer mathematischen Wellengleichungg berechnet werden.
Fazit
Die klassische Physik versagt.....
[Experiment "Körner"]
Interferenz
Elektronen in Atomen müssen als Wellen interpretiert werden, die mit sich selber Interferenz machen. Interferenz entsteht, wenn zwei (oder mehr) Wellen aufeinander treffen. Die Interferenz beschreibt die entstehende Überlagerungserscheinung, das so genannte Interferenzmuster. Grundsätzlich können zwei Typen unterschieden werden:
positive Interferenz
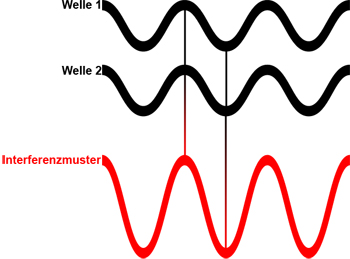
Die erste Möglichkeit der Interferenz ist die so genannte positive oder konstruktive Interferenz. Sie tritt auf, wenn die zwei aufeinandertreffenden Wellen in Phase (die selbe Wellenlänge und am gleichen Ort Maxima bzw. Minima) sind. Die positive Interferenz erzeugt eine verstärkte Welle. Siehe Darstellung unten.
negative Interferenz
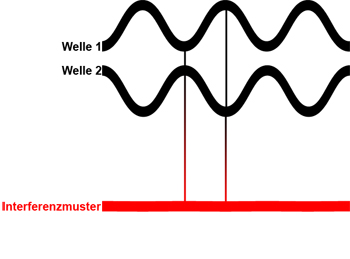
Eine weitere Möglichkeit ist die negative oder destruktive Interferenz. Die Wellen sind in Gegenphase (gleiche Wellenlänge aber Maxima und Minima genau um eine halbe Wellenlänge verschoben). Die negative Interferenz erzeugt eine Auslöschung der Welle. Siehe Darstellung unten.
Interferenz im Alltag
Beispiel: Regenbogenfarben auf Seifenblasenhaut: Licht verschiedener Farben hat bekanntlich verschiedene Wellenlängen.
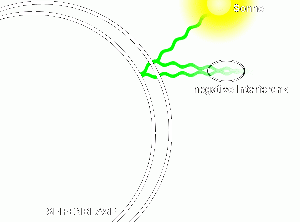
Jeder Lichtstrahl wird bei der Seifenblasenhaut zwei Mal gebrochen (siehe Skizze). Da bei diesen beiden Brechungen der Winkel nicht genau übereinstimmt, treffen die Lichtstrahlen ausserhalb der Seifenblase wieder aufeinander, wo so gezwungenermassen eine Interferenz stattfindet. Wenn nun bei einem bestimmten Abschnitt auf der Seifenblase eine bestimmte Farbe ausgelöscht (durch negative Interferenz) wird, so erscheint der entsprechende Abschnitt in der Komplementärfarbe. Andere Beispiele, bei denen derselbe Vorgang eine Rolle spielt:
- Ölschicht
- Insekten (Flügel oder Panzer)
- CD
Welle-Teilchen-Dualismus
Wenn man Elektronen beobachtet, merkt man, dass sie:
- Wellen (Wahrscheinlichkeitswellen) sind, wenn der Aufenthaltsort nicht genau bestimmt ist.
- Teilchen sind, wenn der Aufenthaltsort bestimmt wird.
Normalerweise ist jedes Physikalische Experiment reproduzierbar. Bei den Elektronen als Teilchen ist dies jedoch nicht so. Das heisst, dass das genau selbe Experiment verschiede Ergebnisse haben kann. Als Beispiel kann man 2 Mal ein Elektron mit genau gleichen Bedingungen auf eine Fläche schiessen und trotzdem erhält man bei den beiden Versuchen verschiede Ergebnisse. Dies hängt mit der Wahrscheinlichkeitsverteilung der Wellengleichung zusammen.
Quellen
- Chemieunterlagen
- Wikipedia