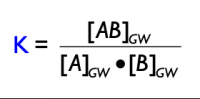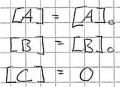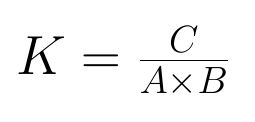Die Beschreibung des Chemischen Gleichgewichts: Unterschied zwischen den Versionen
(→Herleitung Schritt-für-Schritt) |
(→Herleitung Schritt-für-Schritt) |
||
| Zeile 74: | Zeile 74: | ||
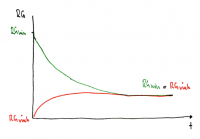
Es ist nötig, das chemische Gleichgewicht mathematisch-quantitativ zu beschreiben, um berechnen zu können, wie groß die Konzentrationen der beteiligten Stoffe im Gleichgewicht sind (z.B. für pH-Wert). Im Kontext der ''Powerpoint Apfelschlacht'' wird dies durch die Gleichung RG = f(k, c) verdeutlicht, wobei im Gleichgewichtszustand gilt: RGhin = RGrück. | Es ist nötig, das chemische Gleichgewicht mathematisch-quantitativ zu beschreiben, um berechnen zu können, wie groß die Konzentrationen der beteiligten Stoffe im Gleichgewicht sind (z.B. für pH-Wert). Im Kontext der ''Powerpoint Apfelschlacht'' wird dies durch die Gleichung RG = f(k, c) verdeutlicht, wobei im Gleichgewichtszustand gilt: RGhin = RGrück. | ||
[[Datei:Graphische Darstellung.png|thumb|left|200px|]] | [[Datei:Graphische Darstellung.png|thumb|left|200px|]] | ||
| + | |||
| + | |||
| + | |||
• Die Grösse der Reaktionsgeschwindigkeit im Gleichgewicht wird ebenfalls durch K beschrieben. | • Die Grösse der Reaktionsgeschwindigkeit im Gleichgewicht wird ebenfalls durch K beschrieben. | ||
Version vom 10. Juni 2024, 23:11 Uhr
Achtung: Diese Seite muss überarbeitet werden - Bitte nicht als Lerngrundlage verwenden!
Inhaltsverzeichnis
1. Das Chemische Gleichgewicht
Definition des Chemischen Gleichgewichts
Ein chemisches Gleichgewicht tritt auf, wenn in einem geschlossenen System die Hin- und Rückreaktionen einer chemischen Reaktion mit derselben Geschwindigkeit ablaufen. Dies bedeutet nicht, dass die chemische Aktivität aufgehört hat, sondern dass sich die Konzentrationen der Reaktanten und Produkte nicht mehr ändern.
Bedeutung des Chemischen Gleichgewichts
Das chemische Gleichgewicht ist ein zentrales Konzept in der Chemie, da es die Dynamik vieler chemischer Reaktionen beschreibt, die in der Natur und in der Industrie stattfinden. Es hilft uns zu verstehen, wie Reaktionen unter bestimmten Bedingungen ablaufen und wie wir diese Bedingungen beeinflussen können, um die Ausbeute an gewünschten Produkten zu maximieren.
Wissenschaftlicher Hintergrund
In einem chemischen Gleichgewicht bleiben die Konzentrationen der Reaktanten und Produkte konstant, obwohl die Reaktionen weiterhin stattfinden. Dies wird durch das Massenwirkungsgesetz beschrieben, das die Beziehung zwischen den Konzentrationen der Reaktanten und Produkte in einem Gleichgewichtszustand angibt:
aA + bB ⇌ cC + dD
2. Der Holzapfelkrieg
Um das Konzept des chemischen Gleichgewichts anschaulich zu erklären, verwenden wir das Beispiel des "Holzapfelkriegs". Dieses Beispiel hilft, den Gleichgewichtsprozesses zu visualisieren.
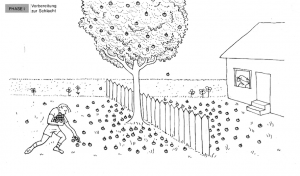
Phase 1: Vorbereitung zur Schlacht
Stellen Sie sich einen Holzapfelbaum vor, der genau auf der Grenze zwischen zwei Gärten steht. In einem Garten wohnt ein Junge, im anderen ein alter Mann. Der Baum trägt viele Holzäpfel, die auf beiden Seiten des Zauns fallen. Zu Beginn sammelt der Junge alle Holzäpfel in seinem Garten auf.
Analogie: Dies entspricht der Sammlung von Reaktanten in einer chemischen Reaktion.
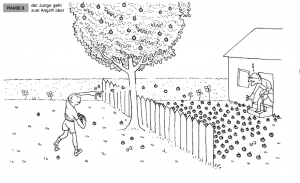
Phase 2: Der Junge geht zum Angriff über
Der Junge möchte die Holzäpfel loswerden und beginnt, sie in den Garten des alten Mannes zu werfen. Der Mann bemerkt dies und beginnt ebenfalls, die Holzäpfel zurückzuwerfen. Die Äpfel werden in beide Richtungen über den Zaun geworfen, wobei zunächst mehr Äpfel im Garten des alten Mannes landen, da der Junge schneller werfen kann.
Analogie: Dies stellt die Hinreaktion dar, bei der die Reaktanten zu Produkten reagieren.
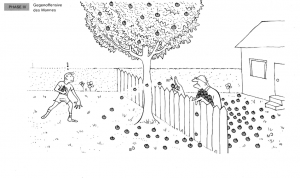
Phase 3: Die Frau beginnt, Äpfel zurückzuwerfen
Die Frau beginnt, die Holzäpfel zurück in den Garten des Jungen zu werfen. Zunächst landen mehr Äpfel im Garten der alten Frau, da der Junge schneller werfen kann.
Analogie: Dies repräsentiert die Rückreaktion, bei der die Produkte wieder zu Reaktanten reagieren.
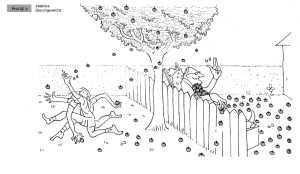
Phase 4: Stabiler Gleichgewichtszustand
Mit der Zeit wirft die Frau genauso viele Äpfel zurück in den Garten des Jungen, wie er in ihren Garten wirft. Es stellt sich ein Gleichgewichtszustand ein, bei dem die Anzahl der Holzäpfel, die in beide Richtungen geworfen werden, gleich ist. Im stabilen Gleichgewichtszustand ändern sich die Mengen an Holzäpfeln in den beiden Gärten nicht mehr, obwohl weiterhin Äpfel hin- und hergeworfen werden.
Analogie: Dies stellt das chemische Gleichgewicht dar, bei dem die Reaktionsgeschwindigkeiten der Hin- und Rückreaktionen gleich sind und die Konzentrationen der Reaktanten und Produkte konstant bleiben.
Wissenschaftlicher Vergleich
In der Chemie entspricht dies einer Situation, in der die Reaktanten A und B zu den Produkten C und D reagieren, bis ein Punkt erreicht ist, an dem die Reaktionsgeschwindigkeiten der Hin- und Rückreaktionen gleich sind:
- A + B ⇌ C + D
Die Konzentrationen der Reaktanten und Produkte bleiben konstant, obwohl die Reaktionen weiterhin stattfinden.
3. das Massenwirkungsgesetzes
Einleitung
Das Massenwirkungsgesetz ist ein fundamentales Prinzip der Chemie, das die Beziehung zwischen den Konzentrationen der Reaktanten und Produkte in einem chemischen Gleichgewicht beschreibt.
Grundprinzipien
Das Massenwirkungsgesetz basiert auf der Beobachtung, dass die Geschwindigkeit einer chemischen Reaktion proportional zu den Konzentrationen der Reaktanten ist. Für eine allgemeine Reaktion der Form:
- aA + bB ⇌ cC + dD
lässt sich das Massenwirkungsgesetz wie folgt formulieren:
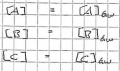
- K = [C]^c [D]^d / [A]^a [B]^b
Hier ist K die Gleichgewichtskonstante, und die eckigen Klammern [] repräsentieren die Konzentrationen der jeweiligen Spezies im Gleichgewichtszustand.
Herleitung Schritt-für-Schritt
Es ist nötig, das chemische Gleichgewicht mathematisch-quantitativ zu beschreiben, um berechnen zu können, wie groß die Konzentrationen der beteiligten Stoffe im Gleichgewicht sind (z.B. für pH-Wert). Im Kontext der Powerpoint Apfelschlacht wird dies durch die Gleichung RG = f(k, c) verdeutlicht, wobei im Gleichgewichtszustand gilt: RGhin = RGrück.
• Die Grösse der Reaktionsgeschwindigkeit im Gleichgewicht wird ebenfalls durch K beschrieben.
• Die Abnahme von RGhin ist der Abnahme der Eduktkonzentrationen proportional
Aussage: Im Zustand des chemischen Gleichgewichts sind die Konzentrationen aller Stoffe konstant, und können mathematisch berechnet werden: Das (mathematische) Produkt der Produktkonzentrationen durch das Produkt der Eduktkonzentrationen ist konstant.
Da khin und krück konstant sind, können sie als neue Konstante zusammengefasst werden --> K: Gleichgewichtskonstante
Massenwirkungsgesetz:
Beispiele
Einführung: Der Holzapfelkrieg
Am besten ist es wohl anhand folgendem Beispiel des Holzapfelkrieges zu verstehen
Man stelle sich einen Holzapfelbaum vor, der auf der Grenzlinie zwischen zwei Gärten steht; in dem einen wohnt eine alte Frau und in dem anderen ein Vater, der seinem Sohn aufgetragen hat, hinauszugehen und den Garten von Holzäpfeln zu reinigen. Der Junge merkt schnell, dass man die Holzäpfel am einfachsten dadurch los wird, wenn man sie in den Nachbargarten wirft. Er tut es und erregt den Zorn der alten Frau. Jetzt beginnen der Junge und die Frau Holzäpfel hin und her, über den Zaun, zu werfen so schnell sie können. Wer wird gewinnen? Die Schlacht läuft in drei Phasen ab. Wenn man annimmt, dass der Junge stärker und schneller ist als die alte Frau, könnte man meinen, dass der Konflikt damit endet, dass alle Äpfel auf der Seite der alten Frau landen . Wenn sich auf beiden Seiten des Zauns die gleiche Anzahl von Äpfeln befindet, ist es zwar richtig, dass der Junge die Äpfel schneller über den Zaun werfen wird, als sie die alte Frau zurückwerfen kann. Aber das heißt nur, dass mehr Äpfel auf der Seite der alten Frau sein werden, die dann leichter zu erreichen sind. Auf der Seite des Jungen werden sie rarer, und der Junge muss mehr herumrennen, um sie aufzuheben. Schließlich wird ein Gleichstand oder ein Gleichgewicht erreicht, in dem die gleiche Anzahl der Äpfel in beiden Richtungen über den Zaun fliegen. Die alten Frau wirft weniger schnell, hat aber geringere Mühe, Äpfel zu finden; der Junge wirft schneller, verliert aber Zeit dadurch, dass er herumrennt und die wenigen Äpfel auf seiner Seite sucht. Das Verhältnis der Äpfel auf den beiden Seiten des Zauns wird schließlich durch die relative Geschwindigkeit der beiden Kämpfer bestimmt, doch werden nicht alle Äpfel auf einer Seite landen.[1]
Die Herleitung des Massenwirkungsgesetzes
Da das Massenwirkungsgesetz von der bestreffenden Reaktionsgleichung abhängig ist, wählen wir ein einfaches Beispiel einer Reaktion:
A + B ⇌ C
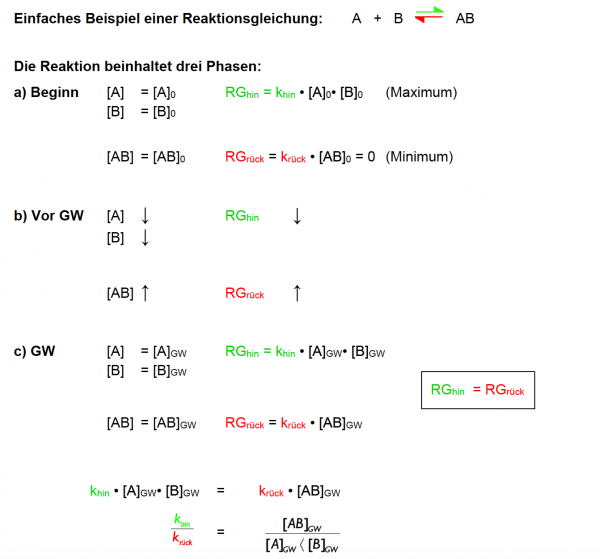
Das Erreichen des chem. Gleichgewichts wird in drei Phasen betrachtet:
- 1. Phase
Bei Beginn, Zeitpunkt 0, gibt es noch keine Produkte und die Edukte sind noch vollzählig.
- 2. Phase
Die Reaktion beginnt, das Produkt wird aus den kleiner werdeden Edukten gebildet.
- 3. Phase
Nun ist das Gleichgewicht erreicht und die Menge der Produkte wie auch der Edukte bleiben gleich, solange nicht etwas anderes das Gleichgewicht stört.
Grundstruktur der Formel
Edukte A und B werden zum Produkt C bis das chemische Gleichgewicht erreicht wird.
A + B ⇌ C
Die Gleichgewichtskonstante
Die Gleichgewichtskonstante K ergibt sich aus dem Division von den Produkten durch die Edukte und gibt Auskunft von welcher Seite mehr vorhanden ist. ( Auf welcher Seite das Gleichgewicht ist.)
K strebt gegen unendlich, wenn fast alle Edukte zu Produkte reagiert haben (Hinreaktion). Somit hat die Konstante K einen Wert von (deutlich)>1. Gibt es nun fast nur Edukte, liegt das GW auf der „linken“ Seite und K ist <1.
Zusammenfassung: Video (Simple Club)
Die Bedeutung des chemischen Gleichgewichts wird am Anfang dieses Video mithilfe eines Beispiels einer einfachen Matherechnung erklärt. Anschließend werden die Verhältnisse der Edukte und der Produkte im Gleichgewicht verdeutlicht. Später kommt man auch auf die Gleichgewichtskonstante K zu sprechen. Dies wird durch ein Beispiel erklärt, in dem eine Reaktion mit den Produkten a und b zu den Edukten c und d reagieren. Hier wird erklärt wie die Hin- und Rückreaktion ausgerechnet werden.
Merke:
- Das chemische Gleichgewicht entsteht bei einer Reaktion bei der nach einer gewissen Zeit die Stoffe, welche als Edukte vorliegen und die Stoffe die als Produkte vorliegen, in einem bestimmten Mengenverhältnis vorliegen.
- Bei einem chemischen Gleichgewicht sind Hin- sowie Rückreaktion gleich schnell.
- Im Unterricht haben wir uns grundsätzlich mit den Bereichen
- K > 1, K < 1 und K = 1 befasst.
- Wenn die Gleichgewichtskonstante (Kc) kleiner als 1 ist, dann liegt das Gleichgewicht auf der linken Seite, also auf der Seite mit den Edukten und wenn es grösser als 1 ist, liegt es auf der rechte Seite, also auf der Seite mit den Produkten.
- Die Gleichgewichtskonstante ist eine Zahl die durch die Division der Konzentration der Produkte und der Konzentration der Edukte entsteht.
- Diese Zahl sagt aus, ob sich das Gleichgewicht schliesslich auf der Seite mit den Edukten oder auf der Seite mit den Produkten befindet.
- Besonders nützlich: Das Video ist einerseits für den Einstieg in das Thema des chemischen Gleichgewichtes nützlich. Andererseits bekommt man einen klaren Einblick und eine klare Erklärung der Gleichgewichtskonstante und deren Zusammenhang mit dem Massenwirkungsgesetz.
Quellen
- Eigene Notizen
Weblinks
- Holzapfelkrieg - Mittlerweile Offline
- Simple Club Video