Säure/Base-Puffer: Unterschied zwischen den Versionen
(→Zusammensetzung) |
(→Puffergleichung von Henderson-Hasselbach) |
||
| Zeile 12: | Zeile 12: | ||
== Puffergleichung von Henderson-Hasselbach == | == Puffergleichung von Henderson-Hasselbach == | ||
| − | Oft braucht man die Puffergleichung von Henderson-Hasselbach zur Berechnung des pH-Wertes von Pufferlösungen. Dadurch lässt sich eine Grafik erstellen, in welcher der pH-Wert in Abhängigkeit zum Verhältnis der korrespondierenden Base | + | Oft braucht man die Puffergleichung von Henderson-Hasselbach zur Berechnung des pH-Wertes von Pufferlösungen. Dadurch lässt sich eine Grafik erstellen, in welcher der pH-Wert in Abhängigkeit zum Verhältnis zwischen der korrespondierenden Base und ihrer Säure dargestellt wird. |
[[Bild:Beispiel.jpg]] | [[Bild:Beispiel.jpg]] | ||
Version vom 18. Juni 2011, 17:51 Uhr
Ein Säure/Base-Puffer ist ein Stoffgemisch, welches in der Lage ist, den pH-Wert einer Lösung trotz Zugabe von Säuren oder Basen annähernd konstant zu halten. Das bedeutet, dass eine grössere Zugabe von Säure oder Base nur eine kleine Änderung des pH-Werts bewirkt.
Inhaltsverzeichnis
Zusammensetzung
Ein Puffer muss so zusammengesetzt sein, dass er die Reaktion der Säure bzw. Base mit Wasser abschwächt. Wird zu der Lösung eine Säure hinzugegeben, muss eine Base vorhanden sein, die an Stelle von Wasser das H+ aufnimmt. Folglich muss das H+ von der Base stärker gebunden werden als von Wasser. Die Base darf jedoch nicht zu stark sein, da sich der pH-Wert sonst erhöht. Analog dazu muss bei Zugabe einer Base eine Säure vorhanden sein, welche an Stelle des Wassers das H+ spendet. Entsprechend gilt, dass das H+ der Säure eher abgegeben wird als das von Wasser. Auch die Säure darf nicht zu stark sein, da ansonsten der pH-Wert verringert wird.
Also verwendet man für den Puffer eine schwache Säure und ihre konjugierte Base. Man beachte, dass die Pufferwirkung eines Säure/Base-Paars im pH-Bereich um dessen pKs-Wert am besten ist.
Puffergleichung von Henderson-Hasselbach
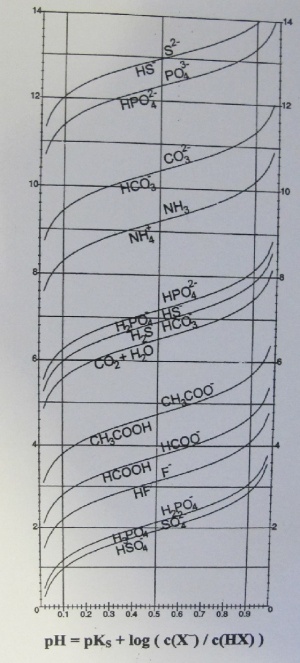
Oft braucht man die Puffergleichung von Henderson-Hasselbach zur Berechnung des pH-Wertes von Pufferlösungen. Dadurch lässt sich eine Grafik erstellen, in welcher der pH-Wert in Abhängigkeit zum Verhältnis zwischen der korrespondierenden Base und ihrer Säure dargestellt wird.
Grafische Darstellung
Die Grafik zeigt, wie der Puffer wirkt. Die Wirkung hat bei relativ grossen Konzentrationsschwankungen eine kleine pH-Wert Veränderung zur Folge. Aus der Grafik kann man erkennen, dass das ideale Verhältnis dann herrscht, wenn der pH-Wert gleich dem pKs-Wert ist, sprich wenn das Verhältnis genau 1 entspricht.
Anwendungsbeispiel
Gegeben: pKs Salzsäure (HCl) : 4.8
Wie ist das Verhältnis, wenn der ph-Wert
a) eine Einheit oberhalb des Pks-Wertes
b) eine Einheit unterhalb des Pks-Wertes liegt?
Quellen
Unterricht von R. Deuber Wikipedia