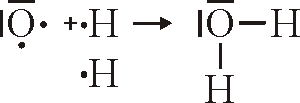Kugelwolkenmodell: Unterschied zwischen den Versionen
| (52 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
| − | + | Zur Beschreibung und Darstellung von Elektronenpaarbindungen wird im Rahmen des Orbitalmodell in der Regel das sogenannte <b>Hybridisierungsmodell</b> verwendet. Dieses ist aber in der druchgehenden Anwendung für den gymnasialen Grundlagenfachunterricht zu anspruchsvoll. | |
| − | |||
| + | Im Folgenden wird deshalb zuerst das Prinzip des Hybridisierungsmodells erklärt, dann aber das <b>Kugelwolkenmodell</b> als stark vereinfachtes - aber durchaus brauchbares Modell - eingeführt. | ||
| − | == Hybridisierung == | + | |
| − | Nähern sich zwei Nichtmetallatome, wirken starke Kräfte: | + | == Hybridisierung - vom Orbitalmodell zum Kugelwolkenmodell == |
| + | Nähern sich zwei Nichtmetallatome, die sich in einer Elektronenpaarbindung verbinden, wirken starke Kräfte: | ||
| + | |||
- Anziehung zwischen den Kernen und den Elektronen des jeweils anderen Atoms | - Anziehung zwischen den Kernen und den Elektronen des jeweils anderen Atoms | ||
| + | |||
- Abstossung zwischen den Elektronen der beiden negativ geladenen Hüllen und den positiv geladenen Kernen | - Abstossung zwischen den Elektronen der beiden negativ geladenen Hüllen und den positiv geladenen Kernen | ||
| − | |||
| − | + | Durch diese Kräfte werden die s- und p-Orbitale räumlich und energetisch so verändert, dass das s-Orbital mit allen 3 p-Orbitalen (sp<sup>3</sup>-Hybridisierung), oder nur mit zwei p-Orbitalen (sp<sup>2</sup>-Hybridisierung) - oder auch nur mit einem p-Orbital (sp-Hybridisierung) verschmilzt. | |
| + | Die dadurch neu entstandenen Orbitale nennt man Hybridorbitale (hybrida (gr): Mischling). | ||
| + | |||
| + | Die gesamte Anzahl Orbitale bleibt dabei gleich: Es sind immer insghesamt 4 Orbitale - entweder 4 Hybridorbitale - oder eine Kombination von Hybridorbitalen und unveränderten p-Orbitalen. | ||
| + | |||
| + | Achtung: Die Zahl im Namen (t.B. sp<b><sub>3</b></sub>) bezieht sich immer auf die Anzahl p- Orbitale, die beteiligt sind - und nicht etwa auf die Anzahl Hybridorbitale! In der sp<sup>3</sup>-Hybridisierung gibt es beispielsweise 4 Hybridorbitale | ||
| + | |||
| + | Im Folgenden wird zuerst die wichtigste Art der sp3-Hybridisierung am Beispiel von Kohlenstoff erklärt, dann noch die seltenere sp<sup>2</sup>- und sp-Hybridisierung. | ||
| + | |||
| + | |||
| + | === sp<sup>3</sup>-Hybridisierung - Beispiel Methan CH<sub>4</sub>=== | ||
| + | |||
| + | Ein einzelnes Kohlenstoffatom weist die folgende Elektronenkonfiguration auf: [He] 2s<sup>2</sup>2p<sup>2</sup> | ||
| + | |||
| + | [[Bild:Hybridisierung_Atomorbitale_col.jpg|400px||Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] | ||
| + | |||
| + | Bei unveränderten Atomorbitalen müsste das Molekül <b>CH<sub>2</sub></b> entstehen! | ||
| + | |||
| + | [[Bild:Hybridisierung_CH2_col.jpg|250px||x]] | ||
| + | |||
| + | |||
| + | Diese Struktur widerspricht aber allen Eigenschaften und experimentellen Analysen von Methan und entspricht damit <b>nicht</b> der Realität - und <b>Die Natur bildet CH<sub>4</sub>, nicht CH<sub>2</sub>!</b> | ||
| + | |||
| + | Warum aber liefert das Orbitalmodell nicht die richtige Struktur? Der Grund liegt darin, dass zusätzlich noch die oben erwähnten Kräfte berücksichtigt werden müssen, welche die Form und Energie der Orbitale verändern! Diese Kräfte führen zu einem energiearmen und symmetrischen Zustand - Eben CH<sub>4</sub>! | ||
| + | |||
| + | Man kann das mathematisch berechnen - wir begnügen uns aber damit, das qualitativ zu beschreiben: | ||
| + | |||
| + | Hat ein Kohlenstoffatom vier Bindungspartner, verschmilzt das s-Orbital mit allen drei p-Orbitalen, wobei vier symmetrische Hybridorbitale entstehen, die gleichmässig um den Kern herum angeordnet sind. Dabei entsteht die bekannte tetraedrische Struktur von Methan: | ||
| + | |||
| + | [[Bild:Hybridisierung_sp3_col.jpg|400px|left|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] [[Bild:Hybridisierung_CH4.jpg|170px|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] | ||
| + | |||
| + | Geometrische Anordnung: tetraedrisch - Bindungswinkel: 109.5° (Tetraederwinkel) | ||
| + | |||
| + | Voraussetzung: Ein sp<sup>3</sup>-hybridisiertes C-Atom hat typischerweise <b>vier Bindungspartner</b>. | ||
| + | |||
| + | |||
| + | === sp<sup>2</sup>-Hybridisierung - Beispiel Ethen C<sub>2</sub>H<sub>4</sub>=== | ||
| + | |||
| + | In Ethen sind die beiden Kohlenstoffe mit je zwei Wasserstoffatomen und gegenseitig mit einer Doppelbindung verbunden: Jedes Kohlenstoffatom hat somit insgesamt <b>drei Bindungspartner</b>. | ||
| + | Da die Anzahl Bindungspartner bei Kohlenstoff jeweils der Anzahl Hybridorbitale entspricht, verschmilzt in diesem Fall das s-Orbital nur mit zwei p-Orbitalen - ein p-Orbital bleibt dabei also unverändert. | ||
| + | |||
| + | [[Bild:Hybridisierung_sp2_col.jpg|400px|left|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] [[Bild:Hybridisierung_Ethen.jpg|320px|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] | ||
| + | |||
| + | |||
| + | |||
| + | |||
| + | <b>Bitte beachten Sie, dass sich die beiden p-Orbitale der beiden sp2-hybridisierten KOhlenstoffatome auch überlappen können!</b>. | ||
| + | |||
| + | Die Bindung besteht aus einem "halben" Orbital oberhalb und einem "halben" Orbital unterhalb. Diese Bindungen werden als"pi-Orbitale" bezeichnet vom griechischen Buchstaben für p, während die Bindungen mit Hybridorbitalen als "sigma-Bindungen" bezeichnet werden vom griechischen Buchstaben für s, da alle aus einem s-Orbial entstanden). In den Darstellungen sind die pi-Orbitale rot, die sigma-Orbitale grün. | ||
| − | + | Beachten Sie auch, dass die pi-Orbitale weniger stark sind als die sigma-Bindungen, da die pi-Elektronen weniger stark von den Kernen angezogen werden (Abstand!). DAs ist der Grund, dass Moleküle mit Doppelbindungen im Allgemeinen reaktionsfreudig sind. | |
| − | + | Geometrische Anordnung: planar-trigonal - Bindungswinkel: 120° | |
| + | Voraussetzung: Ein sp<sup>2</sup>-hybridisiertes C-Atom hat typischerweise <b>drei Bindungspartner</b> (und eine Doppelbindung) | ||
| − | |||
| − | |||
| − | + | === sp-Hybridisierung - Beispiel Ethin C<sub>2</sub>H<sub>2</sub>=== | |
| − | + | In Ethin sind die beiden Kohlenstoffe mit nur je einem Wasserstoffatomen und gegenseitig mit einer Dreifachbindung verbunden: Jedes Kohlenstoffatom hat somit insgesamt nur <b>zwei Bindungspartner</b>. | |
| − | + | In diesem Fall verschmilzt das s-Orbital nur mit zwei p-Orbitalen - ein p-Orbital bleibt dabei also unverändert. Dabei entstehen zwei Hybridorbitale und die beiden p-Orbitale bleiben unverändert | |
| + | [[Bild:Hybridisierung_sp.jpg|400px|left|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] [[Bild:Hybridisierung_Ethin.jpg|320px|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] | ||
| − | |||
| − | + | Wie bei Ethan können sich natürlich auch in diesem Fall die p-Orbitale zu pi-Bindungen überlappen. Diese liegen senkrecht aufeinander und führen zu einer hohen Reaktivität von Alkinen (Kohlenstoffverbindungen mit mindestens einer Dreifachbindung). | |
| − | + | Geometrische Anordnung: linear - Bindungswinkel: 180° | |
| − | |||
| + | Voraussetzung: Ein sp<sup>2</sup>-hybridisiertes C-Atom hat typischerweise <b>zwei Bindungspartner</b> (und zwei Doppelbindungen) | ||
| − | |||
| + | === Zusammenfassung: Hybridisierung=== | ||
| − | + | [[Bild:Hybridisierung Uebersicht col.jpg|800px|Energieniveaus und Orbitale eines einzelnen Kohlenstofftoms]] | |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
== Das Kugelwolkenmodell == | == Das Kugelwolkenmodell == | ||
| − | + | Das Hybridisierungsmodell ist zwar ein sehr leistungsfähiges Modell - aber wie bereits erwähnt - für das Grundlagenfach Chemie in der Schweiz zu anspruchsvoll. | |
| + | Ein einfacheres Modell, das auch in Sekundarschulen bzw. Bezirksschulen verwendet wird, ist das <b>Kugelwolkenmodell</b> | ||
| + | |||
| + | Das Kugelwolkenmodell entspricht im wesentlichen der Vorstellung, dass <b>alle Nichtmetalleatome grundsätzlich sp<sup>3</sup>-hybtridisiert sind</b>, d.h. in der Valenzschale vier Kugelwolken aufweisen, die tetraedrisch um den Kern gruppiert sind. Kugel- oder Elektronenwolken entsprechen im Wesentlichen den sp<sup>3</sup>-Hybridorbitalen. Jedes Atom hat also vier Kugelwolken - und damit insgesamt 4 x 2 = 8 Valenzelektronen | ||
| + | Die Vereinfachung des Kugelwolkenmodells besteht also gewissermassen darin, dass die sp- und sp<sup>2</sup>-Hybridisierung ignoriert werden. Dies ergibt zwar Ungenauigkeiten für Doppelbindungen, mit denen es sich aber leben lässt. | ||
| + | |||
| + | Im Folgenden eine Übersicht der Darstellung von Atomen gemäss Kugelwolkenmodell: | ||
| + | |||
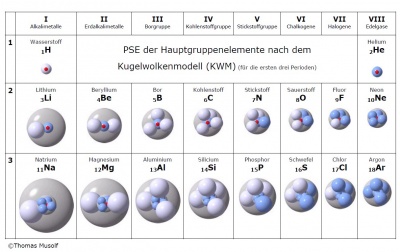
[[Bild:KWM im PS.jpg|thumb|400px|Das KWM im Periodensystem]] | [[Bild:KWM im PS.jpg|thumb|400px|Das KWM im Periodensystem]] | ||
Aktuelle Version vom 24. März 2020, 18:46 Uhr
Zur Beschreibung und Darstellung von Elektronenpaarbindungen wird im Rahmen des Orbitalmodell in der Regel das sogenannte Hybridisierungsmodell verwendet. Dieses ist aber in der druchgehenden Anwendung für den gymnasialen Grundlagenfachunterricht zu anspruchsvoll.
Im Folgenden wird deshalb zuerst das Prinzip des Hybridisierungsmodells erklärt, dann aber das Kugelwolkenmodell als stark vereinfachtes - aber durchaus brauchbares Modell - eingeführt.
Inhaltsverzeichnis
Hybridisierung - vom Orbitalmodell zum Kugelwolkenmodell
Nähern sich zwei Nichtmetallatome, die sich in einer Elektronenpaarbindung verbinden, wirken starke Kräfte:
- Anziehung zwischen den Kernen und den Elektronen des jeweils anderen Atoms
- Abstossung zwischen den Elektronen der beiden negativ geladenen Hüllen und den positiv geladenen Kernen
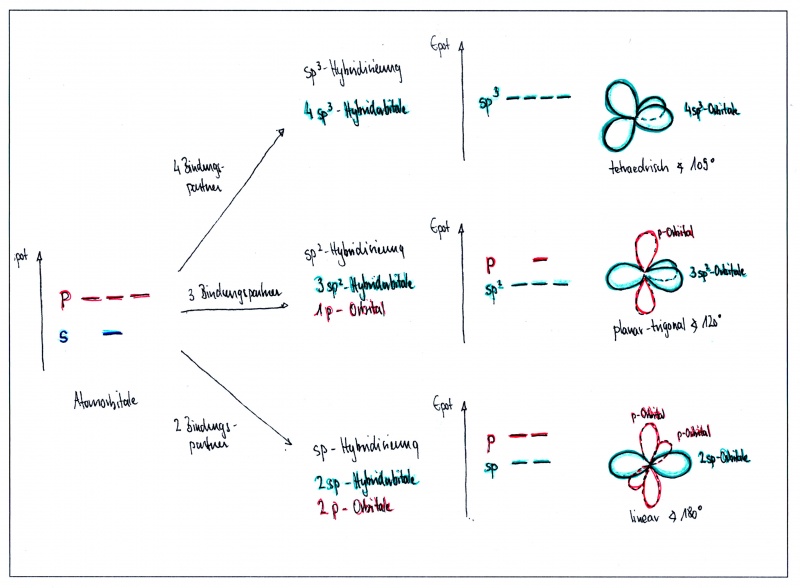
Durch diese Kräfte werden die s- und p-Orbitale räumlich und energetisch so verändert, dass das s-Orbital mit allen 3 p-Orbitalen (sp3-Hybridisierung), oder nur mit zwei p-Orbitalen (sp2-Hybridisierung) - oder auch nur mit einem p-Orbital (sp-Hybridisierung) verschmilzt. Die dadurch neu entstandenen Orbitale nennt man Hybridorbitale (hybrida (gr): Mischling).
Die gesamte Anzahl Orbitale bleibt dabei gleich: Es sind immer insghesamt 4 Orbitale - entweder 4 Hybridorbitale - oder eine Kombination von Hybridorbitalen und unveränderten p-Orbitalen.
Achtung: Die Zahl im Namen (t.B. sp3) bezieht sich immer auf die Anzahl p- Orbitale, die beteiligt sind - und nicht etwa auf die Anzahl Hybridorbitale! In der sp3-Hybridisierung gibt es beispielsweise 4 Hybridorbitale
Im Folgenden wird zuerst die wichtigste Art der sp3-Hybridisierung am Beispiel von Kohlenstoff erklärt, dann noch die seltenere sp2- und sp-Hybridisierung.
sp3-Hybridisierung - Beispiel Methan CH4
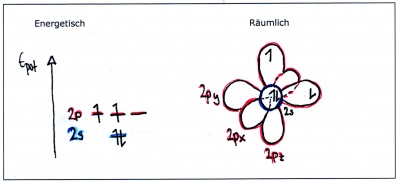
Ein einzelnes Kohlenstoffatom weist die folgende Elektronenkonfiguration auf: [He] 2s22p2
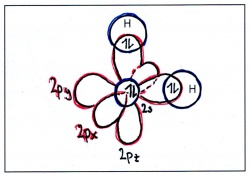
Bei unveränderten Atomorbitalen müsste das Molekül CH2 entstehen!
Diese Struktur widerspricht aber allen Eigenschaften und experimentellen Analysen von Methan und entspricht damit nicht der Realität - und Die Natur bildet CH4, nicht CH2!
Warum aber liefert das Orbitalmodell nicht die richtige Struktur? Der Grund liegt darin, dass zusätzlich noch die oben erwähnten Kräfte berücksichtigt werden müssen, welche die Form und Energie der Orbitale verändern! Diese Kräfte führen zu einem energiearmen und symmetrischen Zustand - Eben CH4!
Man kann das mathematisch berechnen - wir begnügen uns aber damit, das qualitativ zu beschreiben:
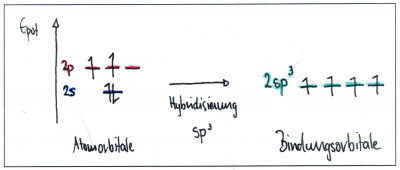
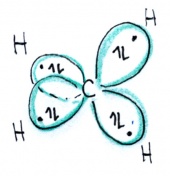
Hat ein Kohlenstoffatom vier Bindungspartner, verschmilzt das s-Orbital mit allen drei p-Orbitalen, wobei vier symmetrische Hybridorbitale entstehen, die gleichmässig um den Kern herum angeordnet sind. Dabei entsteht die bekannte tetraedrische Struktur von Methan:
Geometrische Anordnung: tetraedrisch - Bindungswinkel: 109.5° (Tetraederwinkel)
Voraussetzung: Ein sp3-hybridisiertes C-Atom hat typischerweise vier Bindungspartner.
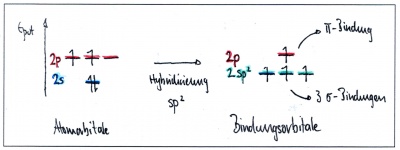
sp2-Hybridisierung - Beispiel Ethen C2H4
In Ethen sind die beiden Kohlenstoffe mit je zwei Wasserstoffatomen und gegenseitig mit einer Doppelbindung verbunden: Jedes Kohlenstoffatom hat somit insgesamt drei Bindungspartner. Da die Anzahl Bindungspartner bei Kohlenstoff jeweils der Anzahl Hybridorbitale entspricht, verschmilzt in diesem Fall das s-Orbital nur mit zwei p-Orbitalen - ein p-Orbital bleibt dabei also unverändert.
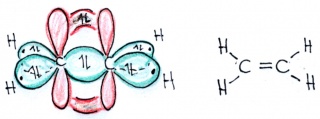
Bitte beachten Sie, dass sich die beiden p-Orbitale der beiden sp2-hybridisierten KOhlenstoffatome auch überlappen können!.
Die Bindung besteht aus einem "halben" Orbital oberhalb und einem "halben" Orbital unterhalb. Diese Bindungen werden als"pi-Orbitale" bezeichnet vom griechischen Buchstaben für p, während die Bindungen mit Hybridorbitalen als "sigma-Bindungen" bezeichnet werden vom griechischen Buchstaben für s, da alle aus einem s-Orbial entstanden). In den Darstellungen sind die pi-Orbitale rot, die sigma-Orbitale grün.
Beachten Sie auch, dass die pi-Orbitale weniger stark sind als die sigma-Bindungen, da die pi-Elektronen weniger stark von den Kernen angezogen werden (Abstand!). DAs ist der Grund, dass Moleküle mit Doppelbindungen im Allgemeinen reaktionsfreudig sind.
Geometrische Anordnung: planar-trigonal - Bindungswinkel: 120°
Voraussetzung: Ein sp2-hybridisiertes C-Atom hat typischerweise drei Bindungspartner (und eine Doppelbindung)
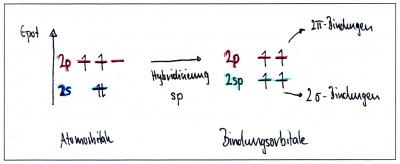
sp-Hybridisierung - Beispiel Ethin C2H2
In Ethin sind die beiden Kohlenstoffe mit nur je einem Wasserstoffatomen und gegenseitig mit einer Dreifachbindung verbunden: Jedes Kohlenstoffatom hat somit insgesamt nur zwei Bindungspartner. In diesem Fall verschmilzt das s-Orbital nur mit zwei p-Orbitalen - ein p-Orbital bleibt dabei also unverändert. Dabei entstehen zwei Hybridorbitale und die beiden p-Orbitale bleiben unverändert
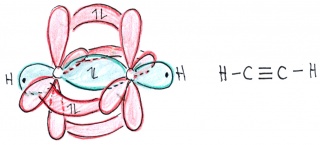
Wie bei Ethan können sich natürlich auch in diesem Fall die p-Orbitale zu pi-Bindungen überlappen. Diese liegen senkrecht aufeinander und führen zu einer hohen Reaktivität von Alkinen (Kohlenstoffverbindungen mit mindestens einer Dreifachbindung).
Geometrische Anordnung: linear - Bindungswinkel: 180°
Voraussetzung: Ein sp2-hybridisiertes C-Atom hat typischerweise zwei Bindungspartner (und zwei Doppelbindungen)
Zusammenfassung: Hybridisierung
Das Kugelwolkenmodell
Das Hybridisierungsmodell ist zwar ein sehr leistungsfähiges Modell - aber wie bereits erwähnt - für das Grundlagenfach Chemie in der Schweiz zu anspruchsvoll. Ein einfacheres Modell, das auch in Sekundarschulen bzw. Bezirksschulen verwendet wird, ist das Kugelwolkenmodell
Das Kugelwolkenmodell entspricht im wesentlichen der Vorstellung, dass alle Nichtmetalleatome grundsätzlich sp3-hybtridisiert sind, d.h. in der Valenzschale vier Kugelwolken aufweisen, die tetraedrisch um den Kern gruppiert sind. Kugel- oder Elektronenwolken entsprechen im Wesentlichen den sp3-Hybridorbitalen. Jedes Atom hat also vier Kugelwolken - und damit insgesamt 4 x 2 = 8 Valenzelektronen Die Vereinfachung des Kugelwolkenmodells besteht also gewissermassen darin, dass die sp- und sp2-Hybridisierung ignoriert werden. Dies ergibt zwar Ungenauigkeiten für Doppelbindungen, mit denen es sich aber leben lässt.
Im Folgenden eine Übersicht der Darstellung von Atomen gemäss Kugelwolkenmodell:
Beispiele zum KWM
Hier folgen zwei Beispiele, an denen man das KWM gut illustrieren und nachvollziehen kann:
|
Wasserstoff (H2): |
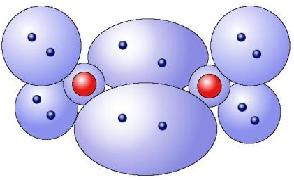
Sauerstoff (O2): |
Grenzen des Modells
Es gibt Unregelmäßigkeiten in der tatsächlichen Besetzung von Schalen bei den Nebengruppenelementen, die sich nur bei einer Annahme erklären lassen: Es muss noch Unterschalen geben. Das lässt sich aber mit dem Kugelwolkenmodell nicht mehr erklären, da es ja nur die jeweils die äusserste Schale betrachtet.
Vergleich: KWM - Orbitalmodell
| Kugelwolkenmodell | Orbitalmodell | |
| gleich | Schalen der Atome | Schalen der Atome |
| Elektronen haben Wellencharakter | Elektronen haben Wellencharakter | |
| Hund'sche Regel, Pauli-Prinzip | Hund'sche Regel, Pauli-Prinzip | |
| verschieden | sp3-Hybridisierung | s/p-Unterschalen |
| Betonung der Valenzschalen | Berücksichtigung aller Schalen | |
| Bindungen der 1. und 2. Periode können gut beschrieben werden, ab der 3. Periode nur eingeschränkt. Nicht geeignet für Nebengruppen, da diese teilweise gleich viele Valenzelektronen haben wie Atome mit anderer Anzahl an Elektronen |
Die Lewisschreibweise
Bei der Lewisschreibweise zeigt man auf einem einfachen weg auf, wieviele Valenzelektronen ein Atom hat, und weiterführend wie die Bindungen zwischen Atomen und Molekülen aussehen. Dabei ersetzt man einfach die vollbesetzetn Kugelwolken durch einen Strich und die einfach besetzten Kugelwolken durch einen Punkt.
Beispiele zur Lewisschreibweise
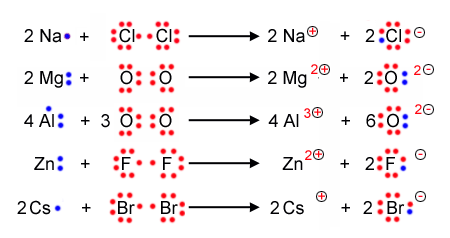
Hier folgen ein paar Beispiele, an denen man die Schreibweie gut illustrieren und nachvollziehen kann:
Bindung von zwei Cl - Atomen
Bindung von H2O
Man kann statt Strichen auch zwei Punkte schreiben:
Quellen
- http://wikipedia.org
- http://google.com
- Heftaufschrieb
- http://www.thomasmusolf.de/fuer_schueler_und_eltern/Chemie/Allgemeines/Wichtige%20Begriffe%20mit%20frame.html
- http://www.bionet.schule.de/~grube/fachlehr/chemie/fundamen/valenz.htm
- http://chemie.fb2.fh-frankfurt.de/Erlaeuterungen/11Hybridisierung-sp3.htm
- http://chemgapedia.de
- http://www.thomasmusolf.de/fuer_schueler_und_eltern/Chemie/Allgemeines/PSE%20-%20online07.jpg
- Elemente-Moleküle; von Roderich Magyar, Wolfgang Liebhart und Gabriela Jelinek