Grundlagen der Ionenbindung: Unterschied zwischen den Versionen
K (1 Version) |
K |
||
| Zeile 1: | Zeile 1: | ||
Die '''[[Grundlagen der Ionenbindung#Die Ionenbindung|Ionenbindung]]'''(siehe auch [[Bildung des Ionengitters]]) entsteht durch die Anziehungskraft zweier unterschiedlich geladener Ionen. Wenn Atome Elektronen aufnehmen oder abgeben, entstehen '''[[Grundlagen der Ionenbindung#Aufbau eines Ions|Ionen]]'''. '''[[Grundlagen der Ionenbindung#Die Ladung eines Ions|Kationen]]''' sind Ionen mit positiver Ladung (aus der [[Valenzschale]] wurden Elektronen abgegeben). '''[[Grundlagen der Ionenbindung#Die Ladung eines Ions|Anionen]]''' sind negativ geladen (in die Valenzschale wurden Elektronen aufgenommen). | Die '''[[Grundlagen der Ionenbindung#Die Ionenbindung|Ionenbindung]]'''(siehe auch [[Bildung des Ionengitters]]) entsteht durch die Anziehungskraft zweier unterschiedlich geladener Ionen. Wenn Atome Elektronen aufnehmen oder abgeben, entstehen '''[[Grundlagen der Ionenbindung#Aufbau eines Ions|Ionen]]'''. '''[[Grundlagen der Ionenbindung#Die Ladung eines Ions|Kationen]]''' sind Ionen mit positiver Ladung (aus der [[Valenzschale]] wurden Elektronen abgegeben). '''[[Grundlagen der Ionenbindung#Die Ladung eines Ions|Anionen]]''' sind negativ geladen (in die Valenzschale wurden Elektronen aufgenommen). | ||
| − | Die Ionenbindung tritt zwischen Metallen und Nichtmetallen (siehe [[Metalle und Nichtmetalle]]) auf. Metalle | + | Die Ionenbindung tritt zwischen Metallen und Nichtmetallen (siehe [[Metalle und Nichtmetalle]]) auf, weil die Metalle ihre Elektronen nur schwach anziehen, die Nichtmetalle hingegen sehr stark. Daher haben Metalle die Tendenz zur Elektronenabgabe, Nichtmetalle die Tendenz zur Elektronenaufnahme. |
Alle Feststoffe, die aus Ionen aufgebaut sind, werden als Salze ([[Eigenschaften von Salzen]]) bezeichnet. | Alle Feststoffe, die aus Ionen aufgebaut sind, werden als Salze ([[Eigenschaften von Salzen]]) bezeichnet. | ||
| Zeile 7: | Zeile 7: | ||
== Aufbau eines Ions == | == Aufbau eines Ions == | ||
| − | Ein Ion besteht aus einem oder mehreren Atomen und | + | Ein Ion besteht aus einem oder mehreren Atomen. Es besitzt eine possitive elektrische Ladung bei der Aufnahme von einem oder mehreren Elektronen und eine negative elektrische Ladung bei der Abgabe von Elektronen. |
Eine Ionenbindung entsteht immer zwischen einem Metall und einem Nichtmetall. | Eine Ionenbindung entsteht immer zwischen einem Metall und einem Nichtmetall. | ||
Sie treten vor allem zwischen Elementen mit hoher [[Elektronegativitätsdifferenz]] auf. (Elemente mit ähnlichen [[Elektronegativitäten]] gehen bevorzugt [[kovalente Bindungen]] ein.) [[image:Ionenbindung_kovalente_Bindung.jpg|middle|Beispiele für Ionenbindung und kovalente Bindung[(Quelle: http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/bindung/ionenbindung.html)] ]] | Sie treten vor allem zwischen Elementen mit hoher [[Elektronegativitätsdifferenz]] auf. (Elemente mit ähnlichen [[Elektronegativitäten]] gehen bevorzugt [[kovalente Bindungen]] ein.) [[image:Ionenbindung_kovalente_Bindung.jpg|middle|Beispiele für Ionenbindung und kovalente Bindung[(Quelle: http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/bindung/ionenbindung.html)] ]] | ||
| Zeile 15: | Zeile 15: | ||
=== Die Ladung eines Ions === | === Die Ladung eines Ions === | ||
| − | Alle Stoffe haben das Bestreben [[Edelgaskonfiguration]] zu erreichen. Bei der Ionenbindung | + | Alle Stoffe haben das Bestreben [[Edelgaskonfiguration]] zu erreichen. Bei der Ionenbindung wird dies erzielt indem das Metall Elektronen abgibt und das Nichtmetall diese aufnimmt. Zugrunde dessen liegt, dass Metalle ihre Elektronen nur schwach anziehen und sie somit die Nichtmetalle problemlos rauben können. Die Edelgaskonfiguration wird also entweder durch die Aufnahme oder die Abgabe von Elektronen aus der Valenzschale erzielt. |
| − | Achtung: | + | Achtung: Die Elektronenverschiebung hat eine Ladungsverschiebung zur Folge und ändert die [[Kernladungszahl]] nicht! |
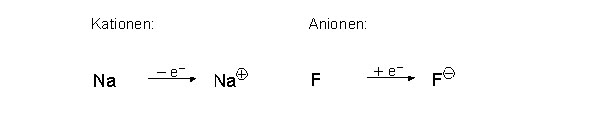
[[image:Kationen_Anionen.jpg|middle|Beispiele für ein Kation und ein Anion;(Quelle: http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/bindung/ionenbindung.html) ]] | [[image:Kationen_Anionen.jpg|middle|Beispiele für ein Kation und ein Anion;(Quelle: http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/bindung/ionenbindung.html) ]] | ||
| Zeile 22: | Zeile 22: | ||
Bei dieser Elektronenverschiebung entstehen positiv und negativ geladenen Teilchen, so genannte Ionen: | Bei dieser Elektronenverschiebung entstehen positiv und negativ geladenen Teilchen, so genannte Ionen: | ||
| − | Positiv geladenen Ionen | + | Positiv geladenen Ionen --> Kationen |
| − | Negativ geladenen Ionen | + | Negativ geladenen Ionen --> Anionen |
| + | |||
[[image:Ionenbindung_Natriumchlorid.jpg|thumb|middle|Natriumchlorid Ion[http://www.uniterra.de/rutherford/kap013.htm)]]] | [[image:Ionenbindung_Natriumchlorid.jpg|thumb|middle|Natriumchlorid Ion[http://www.uniterra.de/rutherford/kap013.htm)]]] | ||
| − | + | Kationen und Anionen sind entweder einfach (Na+ bzw. Cl -), zweifach (Mg 2+ bzw. O2-) oder dreifach (Al3+ bzw. N3-) positiv, respektive negativ, geladen. | |
| − | Generell sind Anionen | + | Generell sind Anionen grösser als Kationen, da durch die Elektronenaufnahme die Valenzschale gefüllt wird und somit das Teilchen sich vergrössert. Im Gegensatz dazu, wird das Kation kleiner, da es durch die Elektronenabgabe eine tiefer gelegene volle Valenzschale erreicht. |
| − | + | Durch die unterschiedliche Ladung der beiden Ionen ziehen sich Kation und Anion gegenseitig an und schliessen sich zu einer Verbindung zusammen. | |
| − | Durch die unterschiedliche Ladung ziehen sich | + | Diese Zusammenlagerung nennt man Ionenbindung. |
| − | |||
== Die Ionenbindung == | == Die Ionenbindung == | ||
Version vom 13. Mai 2010, 17:02 Uhr
Die Ionenbindung(siehe auch Bildung des Ionengitters) entsteht durch die Anziehungskraft zweier unterschiedlich geladener Ionen. Wenn Atome Elektronen aufnehmen oder abgeben, entstehen Ionen. Kationen sind Ionen mit positiver Ladung (aus der Valenzschale wurden Elektronen abgegeben). Anionen sind negativ geladen (in die Valenzschale wurden Elektronen aufgenommen). Die Ionenbindung tritt zwischen Metallen und Nichtmetallen (siehe Metalle und Nichtmetalle) auf, weil die Metalle ihre Elektronen nur schwach anziehen, die Nichtmetalle hingegen sehr stark. Daher haben Metalle die Tendenz zur Elektronenabgabe, Nichtmetalle die Tendenz zur Elektronenaufnahme. Alle Feststoffe, die aus Ionen aufgebaut sind, werden als Salze (Eigenschaften von Salzen) bezeichnet.
Inhaltsverzeichnis
Aufbau eines Ions
Ein Ion besteht aus einem oder mehreren Atomen. Es besitzt eine possitive elektrische Ladung bei der Aufnahme von einem oder mehreren Elektronen und eine negative elektrische Ladung bei der Abgabe von Elektronen.
Eine Ionenbindung entsteht immer zwischen einem Metall und einem Nichtmetall.
Sie treten vor allem zwischen Elementen mit hoher Elektronegativitätsdifferenz auf. (Elemente mit ähnlichen Elektronegativitäten gehen bevorzugt kovalente Bindungen ein.) ![Beispiele für Ionenbindung und kovalente Bindung[(Quelle: http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/bindung/ionenbindung.html)]](/chemiewiki/images/8/8f/Ionenbindung_kovalente_Bindung.jpg)
Die Ladung eines Ions
Alle Stoffe haben das Bestreben Edelgaskonfiguration zu erreichen. Bei der Ionenbindung wird dies erzielt indem das Metall Elektronen abgibt und das Nichtmetall diese aufnimmt. Zugrunde dessen liegt, dass Metalle ihre Elektronen nur schwach anziehen und sie somit die Nichtmetalle problemlos rauben können. Die Edelgaskonfiguration wird also entweder durch die Aufnahme oder die Abgabe von Elektronen aus der Valenzschale erzielt. Achtung: Die Elektronenverschiebung hat eine Ladungsverschiebung zur Folge und ändert die Kernladungszahl nicht!
Bei dieser Elektronenverschiebung entstehen positiv und negativ geladenen Teilchen, so genannte Ionen:
Positiv geladenen Ionen --> Kationen
Negativ geladenen Ionen --> Anionen
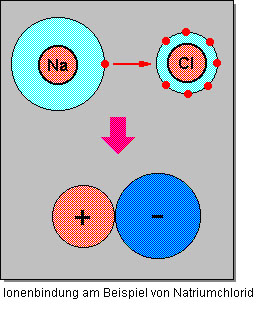
Kationen und Anionen sind entweder einfach (Na+ bzw. Cl -), zweifach (Mg 2+ bzw. O2-) oder dreifach (Al3+ bzw. N3-) positiv, respektive negativ, geladen. Generell sind Anionen grösser als Kationen, da durch die Elektronenaufnahme die Valenzschale gefüllt wird und somit das Teilchen sich vergrössert. Im Gegensatz dazu, wird das Kation kleiner, da es durch die Elektronenabgabe eine tiefer gelegene volle Valenzschale erreicht. Durch die unterschiedliche Ladung der beiden Ionen ziehen sich Kation und Anion gegenseitig an und schliessen sich zu einer Verbindung zusammen. Diese Zusammenlagerung nennt man Ionenbindung.
Die Ionenbindung
Bei einer Ionenbindung wirken zwischen den entgegengesetzt geladenen Ionen elektrostatische Anziehungskräfte, so genannte Coulomb’sche Kräfte. Nach dem coulomb’schen Gesetz ist die Anziehungskraft zwischen zwei elektrischen Ladungen
1. von der Größe der Ladungen
2. vom Abstand zwischen den Ladungen abhängig.
Da die gegenseitige Anziehung in alle Richtungen gleich stark wirkt, umlagern sich entgegengesetzt geladene Ionen zu einem geordneten Aufbau in einer Verbindung. Es bildet sich ein so genanntes Ionengitter (ein Kristall) mit der typischen Gitterstruktur. Das Ionengitter (Bildung des Ionengitters) ist elektrisch neutral, da sich die entgegengesetzten Ladungen gegenseitig aufheben. Voraussetzung ist die korrekte stöchiometrische Zusammensetzung der kleinsten chemischen Einheit.
Quellen
- Chemieunterlagen
Weblinks
- Uni Erlangen - Ionenbindungen und kovalente Bindungen
- Uniterra - Natriumchlorid