Katalyse: Unterschied zwischen den Versionen
| Zeile 27: | Zeile 27: | ||
Die einzelnen Teilschritte (Reaktion mit einem Katalysator) brauchen weniger Energie und somit hat eine grössere Anzahl Teilchen die erforderliche Mindestenergie zur Reaktion. Beide Teilreaktionen verlaufen schneller, somit auch die Gesamtreaktion. | Die einzelnen Teilschritte (Reaktion mit einem Katalysator) brauchen weniger Energie und somit hat eine grössere Anzahl Teilchen die erforderliche Mindestenergie zur Reaktion. Beide Teilreaktionen verlaufen schneller, somit auch die Gesamtreaktion. | ||
| + | |||
| + | == Heterogene / Homogene Katalyse == | ||
| + | |||
| + | Es gibt zwei verschiedene Arten von Katalyse, die heterogene und die homogene Katalyse. | ||
| + | |||
| + | Bei der heterogenen Katalyse unterscheidet sich der Aggregatszustand des Katalysators vom Aggregatszustand der reagierenden Stoffe. Der Katalysator ist hierbei meist ein Feststoff. Dies erleichtert das Abtrennen des Katalysators vom Reaktionsgemisch nach der Reaktion. | ||
| + | |||
| + | Bei der homogenen Katalyse befinden sich der Katalysator wie auch der reagierende Stoff im gleichen Aggregatszustand. Das hat den Vorteil, dass es mildere Reaktionsbedingungen benötigt (z.B. niedriger Druck). Jedoch ist die Trennung des Katalysators vom Reaktionsgemisch erschwert. | ||
| + | |||
| + | |||
| + | |||
| + | == Quellen == | ||
| + | http://www.google.ch/imgres?q=katalyse&num=10&hl=de&tbo=d&tbm=isch&tbnid=COYzTx3PbClLTM:&imgrefurl=http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/4/cm/kinetik/einf_kat.vlu/Page/vsc/de/ch/4/cm/kinetik/katalyse2.vscml.html&docid=9o-8DUxLW8lcAM&imgurl=http://www.chemgapedia.de/vsengine/media/vsc/de/ch/4/cm/kinetik/bilder/profil2.gif&w=591&h=371&ei=Hkn5UJvpOsXTsgaOoYG4AQ&zoom=1&iact=rc&dur=1&sig=108609485422497529777&page=1&tbnh=139&tbnw=221&start=0&ndsp=20&ved=1t:429,r:3,s:0,i:105&tx=81&ty=37&biw=1366&bih=673 | ||
| + | http://www.pci.tu-bs.de/aggericke/PC5-Grenzf/Heterogene%20Katalyse.pdf | ||
Version vom 18. Januar 2013, 14:38 Uhr
Inhaltsverzeichnis
Was ist eine Katalyse?
Als Katalyse bezeichnet man die Beschleunigung einer Reaktion durch einen Katalysator. Katalysatoren sind Stoffe die sich zur Beschleunigung einer Reaktion einsetzen lassen, wobei sie selbst nicht verbraucht werden.
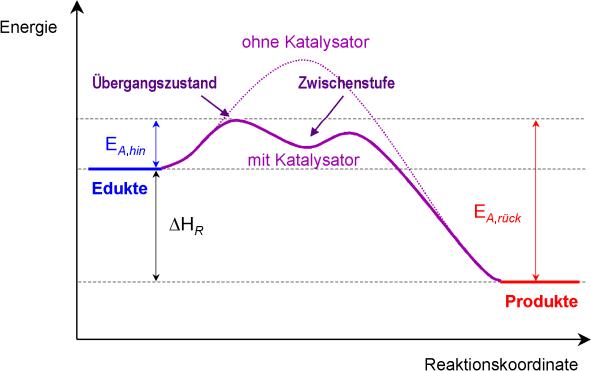
Energiediagramm:
Übergangszustand: Bindung an den Katalysator
Zwischenstufe: Lösen vom Katalysator und Bindung mit dem eigentlichen Teilchen
Schlussfolgerung: Mit einem Katalysator braucht man wesentlich weniger Aktivierungsenergie.
Wie funktioniert ein Katalysator?
Der Katalysator geht mit einem der Edukte eine Zwischenbindung ein. Er schwächt die zwischenmolekularen Kräfte des Eduktes und so kann das geschwächte Edukt mit weniger Energie mit dem anderen Edukt reagieren. Am Schluss hat man das Produkt und den wieder freigewordene Katalysator.
Ohne Katalysator: A + B => AB braucht viel Energie
Mit Katalysator: A + K(atalysator) => AK und AK + B => AB + K weniger Energie
Die einzelnen Teilschritte (Reaktion mit einem Katalysator) brauchen weniger Energie und somit hat eine grössere Anzahl Teilchen die erforderliche Mindestenergie zur Reaktion. Beide Teilreaktionen verlaufen schneller, somit auch die Gesamtreaktion.
Heterogene / Homogene Katalyse
Es gibt zwei verschiedene Arten von Katalyse, die heterogene und die homogene Katalyse.
Bei der heterogenen Katalyse unterscheidet sich der Aggregatszustand des Katalysators vom Aggregatszustand der reagierenden Stoffe. Der Katalysator ist hierbei meist ein Feststoff. Dies erleichtert das Abtrennen des Katalysators vom Reaktionsgemisch nach der Reaktion.
Bei der homogenen Katalyse befinden sich der Katalysator wie auch der reagierende Stoff im gleichen Aggregatszustand. Das hat den Vorteil, dass es mildere Reaktionsbedingungen benötigt (z.B. niedriger Druck). Jedoch ist die Trennung des Katalysators vom Reaktionsgemisch erschwert.
Quellen
http://www.google.ch/imgres?q=katalyse&num=10&hl=de&tbo=d&tbm=isch&tbnid=COYzTx3PbClLTM:&imgrefurl=http://www.chemgapedia.de/vsengine/vlu/vsc/de/ch/4/cm/kinetik/einf_kat.vlu/Page/vsc/de/ch/4/cm/kinetik/katalyse2.vscml.html&docid=9o-8DUxLW8lcAM&imgurl=http://www.chemgapedia.de/vsengine/media/vsc/de/ch/4/cm/kinetik/bilder/profil2.gif&w=591&h=371&ei=Hkn5UJvpOsXTsgaOoYG4AQ&zoom=1&iact=rc&dur=1&sig=108609485422497529777&page=1&tbnh=139&tbnw=221&start=0&ndsp=20&ved=1t:429,r:3,s:0,i:105&tx=81&ty=37&biw=1366&bih=673 http://www.pci.tu-bs.de/aggericke/PC5-Grenzf/Heterogene%20Katalyse.pdf