Die polare Bindung: Unterschied zwischen den Versionen
K |
|||
| Zeile 51: | Zeile 51: | ||
| − | Die Elektronegativität (ΔEN) wird folgendermassen ausgerechnet: | + | '''Die Elektronegativität (ΔEN) wird folgendermassen ausgerechnet:''' |
ΔEN = EN<SUB>Atom 1</SUB>- EN<SUB>Atom 2</SUB> | ΔEN = EN<SUB>Atom 1</SUB>- EN<SUB>Atom 2</SUB> | ||
Version vom 29. Mai 2010, 12:28 Uhr
Exp:
Pentan → brennbar : energiereich
Wasser → nicht brennbar : energiearm
Bei der polaren Atombindung nutzen zwei oder mehrere Nichtmetalle ihre Valenzelektronen gemeinsam, um die energetisch günstige Edelgaskonfiguration anzustreben. Dabei geschieht es, dass die gemeinsamen Bindungselektronen stärker vom Atom mit der höheren Elektronegativität angezogen werden. Dadurch erfährt das Molekül eine Polarisierung.
Polare Stoffe lösen sich besser in polaren Lösungsmittel (z.B. Salze in Wasser). Die Löslichkeit ist umso besser, je ähnlicher die Wechselwirkungskräfte zwischen den Teilchen des Lösungsmittels und zwischen denen des gelösten Stoffes sind. (siehe: Löslichkeit)
Inhaltsverzeichnis
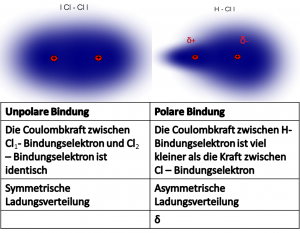
Polare-unpolare Bindung
Im Chlormolekül liegen zwei gleiche Atome vor:
Sie haben beide die gleiche Kernladung und die gleiche Größe.
→ sie haben dieselbe Elektronegativität (EN)
→ die Bindungselektronen sind gleichmässig zwischen den Atomen verteilt
→die Atombindung ist unpolar
Im Chlorwasserstoffmolekül liegen zwei unterschiedliche Atome vor:
Wasserstoff hat eine geringe Kernladung und ist ein kleines Atom → geringe EN (2,2)
Das Chloratom hat eine höhere Kernladung als Wasserstoff und ist auch größer → höhere EN (3.2)
Da Chlor das elektronegativere Atom ist, zieht es die Bindungselektronen etwas näher zu sich.
→ die Bindungselektronen sind ungleichmäßig verteilt.
→ die Atombindung ist polar.
Die Elektronegativität
Definition
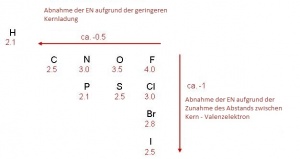
Die Elektronegativität (ΔEN) ist ein Mass für die Anziehungskraft die ein Atomkern in einer Molekülbinung auf die Elektronenpaare ausübt. Die Elektronegativität nimmt in einer Periode von links nach rechts zu, weil die Anzahl der Protonen im Kern steigt. In einer Gruppe nimmt die Elektronegativität von oben nach unten ab, da der Abstand zwischen Elektron und Atomkern zunimmt. Dieses Konzept wurde von Linus Pauling [1] im Jahr 1932 ingeführt.
Alle Stoffe streben danach die Edelgaskonfiguration zu erreichen. Die Metallatome geben ihre Elektronen ab, die Nichtmetalle nehmen diese Elektronen auf. Dabei entsteht eine Ionenbindung (Nichtmetall - Metall). (siehe:Grundlagen der Ionenbindung)
→ Bei den Edelgasen gibt es keine Elektronegativität, da sie bereits volle Valenzelektronenschale haben.
Die Elektronegativität (ΔEN) wird folgendermassen ausgerechnet:
ΔEN = ENAtom 1- ENAtom 2
Faustregel: Eine Bindung ist dann polar, wenn ΔEN > 0.5
Die Stärke der polaren Bindung
Die polare Bindung ist die stärkste Elektronenpaarbindung und somit auch die stärkste Bindung zwischen zwei Nichtmetallen.
→ polare Bindungen sind starke Bindungen, da es viel Energie braucht, um dem elektronegativen Atom das Elektron des Bindiungspartners wieder wegzunehmen.
→ polare Bindungen sind leicht zu bilden
→ bei der Bildung der Bindung wird Energie frei
Quellen
-Chemie-Unterricht Notitzen
-Graphics made by Urs Wegmann